精准引领,双维突破:2026 ASCO GI转移性结直肠癌生物标志物驱动治疗新进展
引言
精准医学的纵深发展正在重新定义转移性结直肠癌的治疗格局。随着分子病理学的进步,以RAS、BRAF、HER2、MMR等为代表的可靶向生物标志物相继被发现,为患者提供了更为个体化的治疗选择。然而,在真实世界的临床实践中,生物标志物检测的普及性与规范性仍面临挑战,尤其是在资源有限的社区医疗环境中,检测不足、延迟或漏检等问题普遍存在,直接制约了精准治疗的落地。与此同时,抗EGFR单抗在RAS/BRAF野生型患者中的应用在中国已走过二十余年历程,耐药后的再挑战策略在循环肿瘤DNA(ctDNA)技术的赋能下重新焕发生机,为后线治疗提供了新的思路。2026年ASCO GI年会上发布的两项研究——转移性结直肠癌的生物标志物驱动及循证治疗(BEAT-CRC)平台的真实世界实践与ctDNA指导下的西妥昔单抗再挑战临床试验,分别从系统优化和分子筛选两个维度,回应了精准医疗在临床转化中的关键瓶颈,展现了生物标志物驱动治疗从理念到实践的双重跃迁。
转移性结直肠癌的生物标志物驱动及循证治疗(BEAT-CRC):一项旨在提升大型临床实践网络中生物标志物驱动治疗可及性的全系统计划1
研究概述
结直肠癌是全球第二大癌症死亡原因,其中超过90%的死亡由转移性病变引起。超过50%的转移性结直肠癌患者携带可靶向的生物标志物,包括RAS(50–60%)、BRAF(10%)、MMRd/MSI-H(4%)及ERBB2/HER2(3%)。尽管指南推荐进行生物标志物检测,但在真实世界临床实践中,尤其是在社区医疗环境中,执行率仍不理想。鉴于此,本研究提出假设:通过实施BEAT-CRC平台,能够提高生物标志物检测率,并促进更多样化的患者群体接受生物标志物指导的治疗。研究采用前瞻性干预设计,在大学医院赛德曼癌症中心这一大型混合型学术-社区网络中,集成了基于电子病历(EMR)的自动追踪模块。该模块可实时监测患者的生物标志物检测状态,自动触发缺失检测项目的启动,并向临床医生推送提示信息,以指导生物标志物驱动的治疗决策。通过对干预前后检测率的比较分析,评估BEAT-CRC平台在真实世界实践中的实施效果。
图. 从组织样本接收、生物标志物检测到治疗实施的全新BEAT-CRC工作流
研究结果
2024年5月至2025年9月期间,共筛选900例病例,其中143例被确诊为转移性结直肠癌并纳入分析。基线检测率显示:MMR IHC为99%,NGS为87%,HER2检测仅为17%。干预后,HER2检测率提升了5倍以上(绝对增长72%),NGS检测率也略有上升(增长3%)。在生物标志物阳性率方面,BRAF V600E为5%,RAS/RAF突变为53%,KRAS G12C为2%,HER2阳性为2%,dMMR为8%。结果表明,基于EMR的集成模块能够在大型混合型学术-社区网络中显著提高治疗前生物标志物检测率。
图. 基线和干预后的检测率(N=143)
研究结论
BEAT-CRC平台在真实世界临床实践中有效提升了生物标志物检测率,尤其是在HER2检测方面取得了显著进展。未来研究应进一步明确检测率的提升是否转化为更多患者接受生物标志物驱动的治疗,并评估该举措是否能增强患者对生物标志物及基因检测必要性的认知。此外,BEAT-CRC平台有望助力提升临床试验的可及性,推动精准治疗在社区实践中的落地。
ctDNA指导西妥昔单抗联合伊立替康再挑战用于中国RAS/BRAF野生型转移性结直肠癌患者2
研究概述
抗EGFR再挑战治疗作为延长RAS/BRAF野生型转移性结直肠癌患者治疗周期的新兴策略,近年来受到广泛关注。治疗前ctDNA分析可通过识别并排除存在获得性耐药突变的患者,实现分子指导下的精准筛选。本研究是一项在中国开展的多中心、单臂、Ⅱ期临床试验,旨在通过ctDNA前瞻性筛选既往经西妥昔单抗一线治疗获益(客观缓解或疾病稳定≥6个月)、后线治疗中未再使用抗EGFR药物且疾病进展后停用西妥昔单抗至少4个月、同时ctDNA检测仍维持RAS/BRAF野生型状态的患者,评估西妥昔单抗联合伊立替康再挑战治疗的疗效和安全性。主要终点为客观缓解率,次要终点包括PFS、OS及治疗相关不良事件。
研究结果
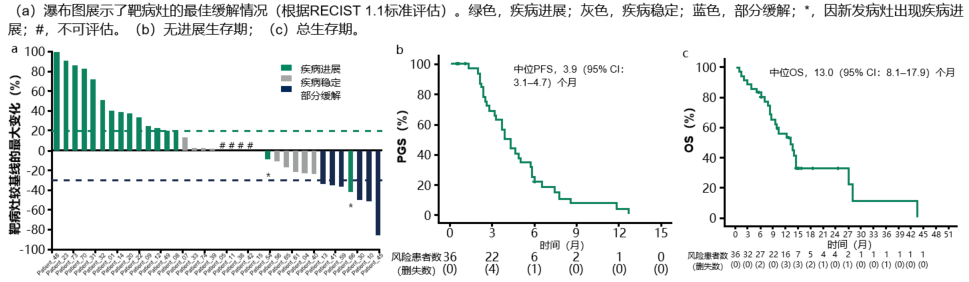
研究自2019年11月至2025年2月共纳入36例患者,其中32例完成疗效评估。在意向治疗人群中,客观缓解率为16.7%(95%CI: 5.6-27.8),疾病控制率为44.4%(95%CI: 27.8-61.1)。中位PFS为3.9个月(95%CI: 3.1–4.7),中位OS为13.0个月(95%CI: 8.1–17.9)。单变量及多变量分析均显示,西妥昔单抗停药至研究筛查的时间间隔与PFS显著相关(P=0.004和P=0.013)。基于两倍半衰期将时间间隔分为三组(<8个月、8-16个月、>16个月),结果显示长间隔组患者的PFS更长。安全性方面,3-4级治疗相关不良事件包括皮疹(8.3%)、中性粒细胞减少症(8.3%)、贫血(5.6%)和腹泻(2.8%),整体耐受性良好。
图. 肿瘤缓解情况及Kaplan-Meier估计值
研究结论
对于既往经西妥昔单抗治疗获益、后线治疗中仍维持RAS/BRAF野生型状态的中国转移性结直肠癌患者,经ctDNA筛选后接受西妥昔单抗联合伊立替康再挑战治疗,显示出一定的抗肿瘤活性和可接受的安全性。该研究为抗EGFR再挑战策略在精准医学时代的临床应用提供了前瞻性证据,提示ctDNA指导下的分子筛选有望优化患者选择,延长治疗获益周期。
结语
从系统级的流程重构到个体化的分子筛选,上述两项研究共同勾勒出转移性结直肠癌精准治疗的前沿图景。BEAT-CRC平台通过嵌入电子病历的自动化模块,显著提升了生物标志物检测率,证明在真实世界环境中,精准医疗的推广不仅依赖于新药的研发,更有赖于诊疗流程的数字化和智能化改造。而ctDNA指导下的西妥昔单抗再挑战研究,则在后线治疗领域提供了“老药新用”的精准范本,证实分子动态监测可有效筛选获益人群,延长治疗窗口。二者虽切入角度不同,却殊途同归——都在回答同一个核心命题:如何让对的治疗,在对的时间,给到对的患者。未来,随着检测技术的进一步普及与临床决策支持系统的完善,精准医学将在更大范围内从“可及”走向“可控”,从“证据”走向“实践”。
编辑林颖整理

所有文章未经授权禁止转载、摘编、复制或建立镜像,违规转载法律必究。
举报邮箱:1002263188@qq.com