连发Nature、 ACS Catalysis,二价铑催化剂用量可低至0.0005 mol%!
C-H functionalization
近年来C-H官能化方法取得重大突破,但对于简单环己烷体系,尤其是电中性且结构对称的底物,实现精准选择仍然困难。既有策略如卡宾插入、氧化反应及自由基过程在一定程度上能够实现转化,但普遍存在区域选择性和立体控制较差的问题。因此,通过催化剂本身调控反应位点,从而超越底物固有反应性的限制,被视为一种极具潜力的策略。
2018年,Huw M. L. Davies课题组基于手性二铑催化剂体系的发展,利用供体/受体卡宾插入反应,实现了对环己烷衍生物的高选择性去对称化。
条件筛选发现新开发的Rh2(S-TPPTTL)4催化剂表现出显著优势,不仅能够在多个潜在反应位点中精确控制反应位点,还能在单一步骤中构建多个立体中心,体现出优异的不对称诱导能力。
Ultra-high catalytic efficiency
毕得Rh2(TPPTTL)4催化剂
点击结构查看产品详情
BD02625362
BD02571380
在以叔丁基环己烷为模型底物时,尽管体系中存在多种可反应C-H键,该催化剂仍能高度选择性地在C3位发生插入反应,区域选择性超过50:1,对映选择性达到95%。进一步的底物范围研究表明,该催化体系对多种环烷烃及取代环己烷均具有良好适用性。不同取代基尺寸对反应结果产生显著影响:随着取代基体积增大,非对映选择性明显提升,显示出更强的去对称化效应。同时,反应对侧链C-H键表现出显著抑制,即使这些位点在空间上更易接近,也仅生成痕量副产物。此外,多种芳基重氮化合物均可作为卡宾前体参与反应,但其对位取代基的位阻会对对映选择性产生一定影响。
在更复杂体系中,二取代环己烷的反应进一步揭示了位阻与构象对反应选择性的影响。对于存在椅式构象互变的底物,反应通常在不同构象间同时进行,从而导致非对映选择性降低。对轴向与平伏C-H键反应性的比较表明,平伏位点具有显著优势,其反应速率可高出两个数量级以上。该选择性远高于以往报道的类似体系,体现出催化剂在空间识别方面的高度精细调控能力。扩展至稠环体系如十氢萘时,反应同样能够高效进行,进一步验证了该方法的普适性。
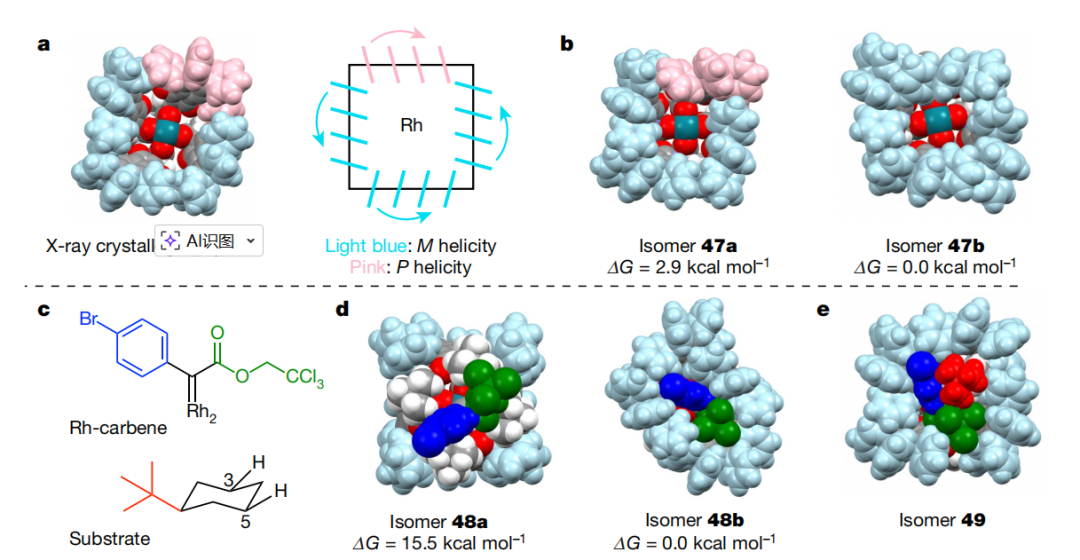
结构研究与理论计算能解释反应的高选择性。X射线晶体学分析显示,该催化剂具有由四个配体构成的“手性冠状”结构,多个苯基呈现协同倾斜排列,形成类似螺旋桨的整体手性环境。计算结果表明,这种配体取向在能量上更稳定,并在卡宾结合及底物进入过程中发挥关键作用。催化剂在反应过程中表现出显著的构型适应性,可根据卡宾和底物的接近方式发生结构调整,从而实现类似“诱导契合”的动态匹配。
对反应过渡态的分析进一步表明,位点选择性主要源于底物取代基与催化剂“口袋”之间的空间匹配关系。对于叔丁基环己烷,最有利的构型是使体积较大的取代基远离催化剂内部拥挤区域,从而引导特定平伏C-H键靠近活性卡宾中心,实现高度选择性的插入过程。这种精细的空间识别能力使催化剂能够区分原本等同的C-H键,从而实现真正意义上的去对称化。
Nature 2018, 564, 395.
2019年,Huw M. L. Davies课题组又利用二价铑Rh2(S-TPPTTL)4为催化剂,通过芳基重氮乙酸酯生成的供体/受体卡宾,实现有机硅烷sp3 C-H键的区域选择性与立体选择性官能化。
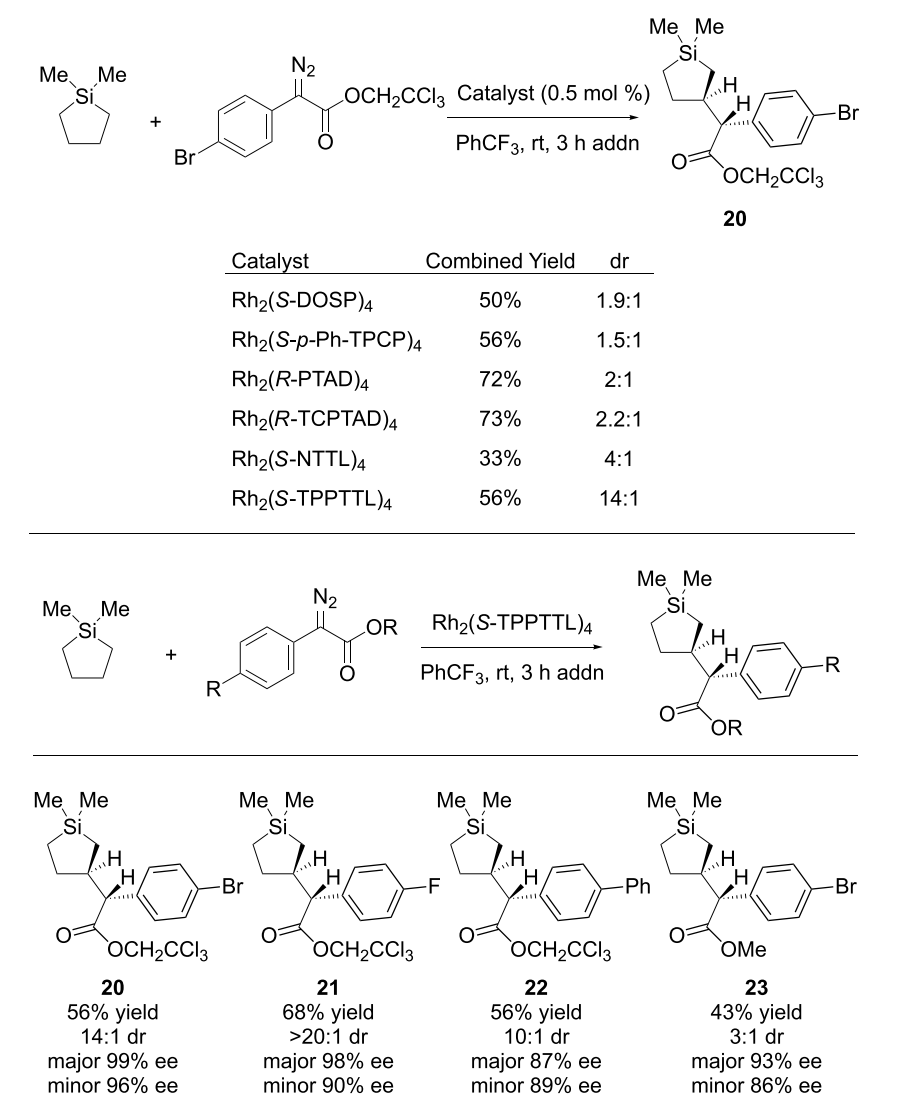
底物普适性研究表明,多种取代芳基重氮乙酸酯均可参与反应,包括含杂芳环(如吡啶、嘧啶和噻吩)的底物,均能保持较高对映选择性。对于硅杂环底物,尽管较大位阻的芳基可能降低收率,但整体反应表现出良好的普适性。X射线晶体学分析确认了产物的绝对构型。
在五元硅杂环体系中,Rh2(S-TPPTTL)4表现出显著优于其他催化剂的非对映选择性控制能力,同时保持高对映选择性。对比不同酯基发现,三氯乙酯在提高非对映选择性方面具有关键作用。该催化体系还可有效调控轴向与赤道C-H键的选择性官能化,在部分底物中实现超过20:1的非对映选择性,并保持优异的对映控制。
Org. Lett. 2019, 21, 4910.
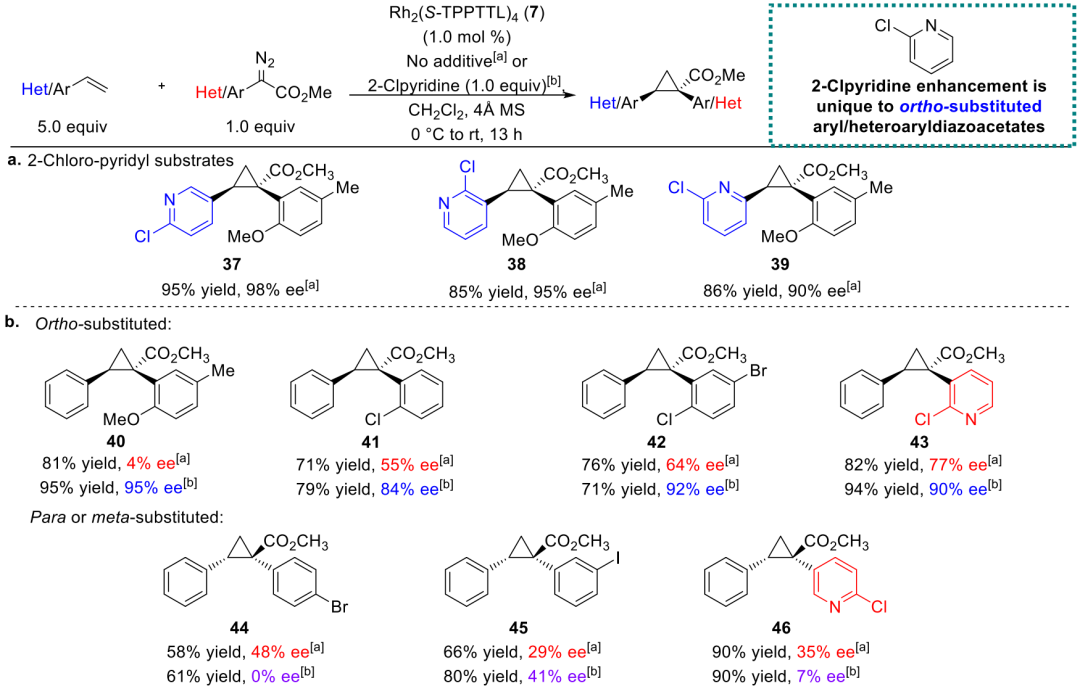
Huw M. L. Davies课题组,2021年继续利用二价铑催化剂Rh2(S-TPPTTL)4解决邻位取代芳基重氮乙酸酯反应选择性差的问题。
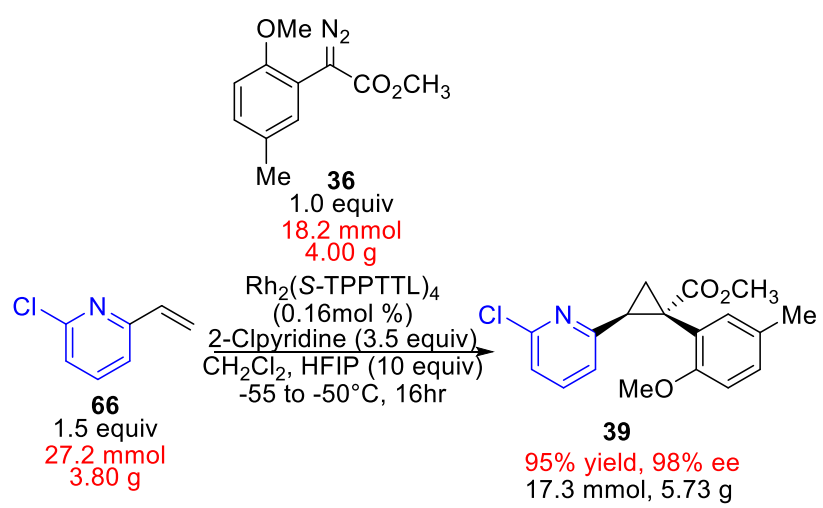
底物拓展显示,在Rh2(S-TPPTTL)4/2-氯吡啶体系下,多种乙烯基杂环均可高效参与反应,生成环丙烷产物,普遍具有86->99% ee,体现出良好的底物兼容性。同时,以HFIP替代大量分子筛可维持高选择性并简化操作,使反应可在克级规模下进行且降低催化剂用量。
ChemRxiv, 2021, 10.26434/chemrxiv.14479593.v1.
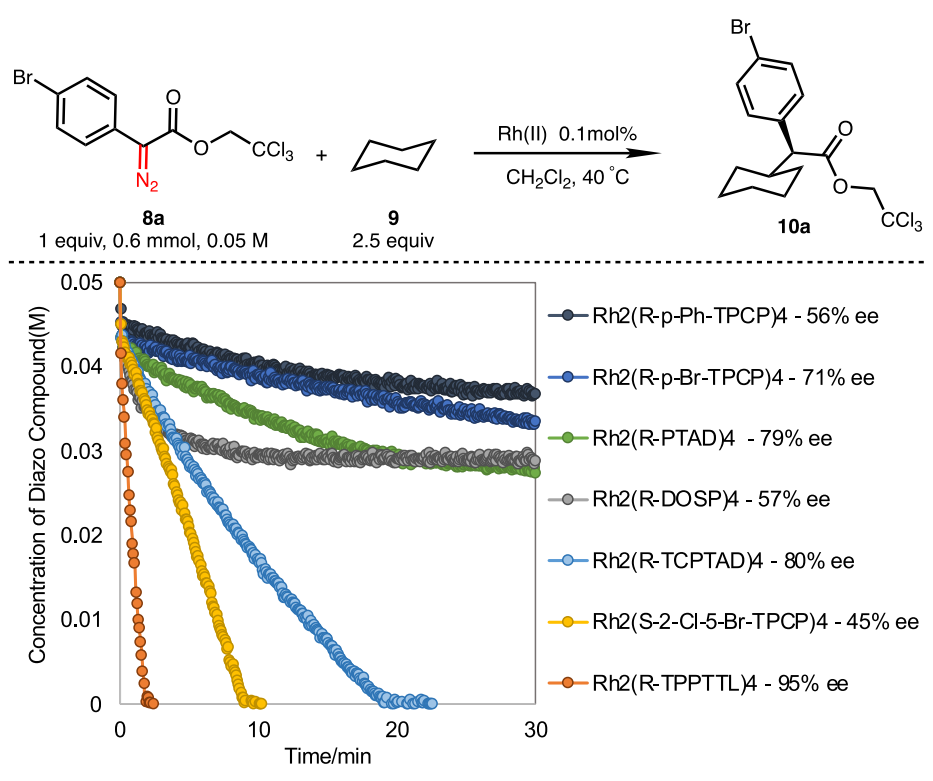
2022年,Huw M. L. Davies课题组再次利用二价铑催化剂Rh2(R-TPPTTL)4催化芳基重氮乙酸酯与未活化烃类sp3 C-H键的官能化反应。通过原位动力学分析对反应进行考察,希望提升反应效率并实现超高催化剂周转数(TON)。
动力学与计算研究表明,该反应机理不同于环丙烷化反应:在C-H官能化过程中,卡宾插入步骤而非卡宾生成步骤为速率决定步骤。实验通过反应进程动力学分析(RPKA)证实,反应对烃底物和催化剂呈正级数,对重氮化合物呈零级数,符合Michaelis-Menten行为。这意味着提高C-H键捕获效率是提升整体反应速率的关键。
催化剂筛选显示,具有C4对称“碗状”结构的Rh2(R-TPPTTL)4表现最佳,可在短时间内实现高转化率与优异对映选择性(约95% ee)。相比之下,其他常用于环丙烷化的催化剂在该体系中表现不佳,说明催化剂结构对反应路径具有决定性影响。
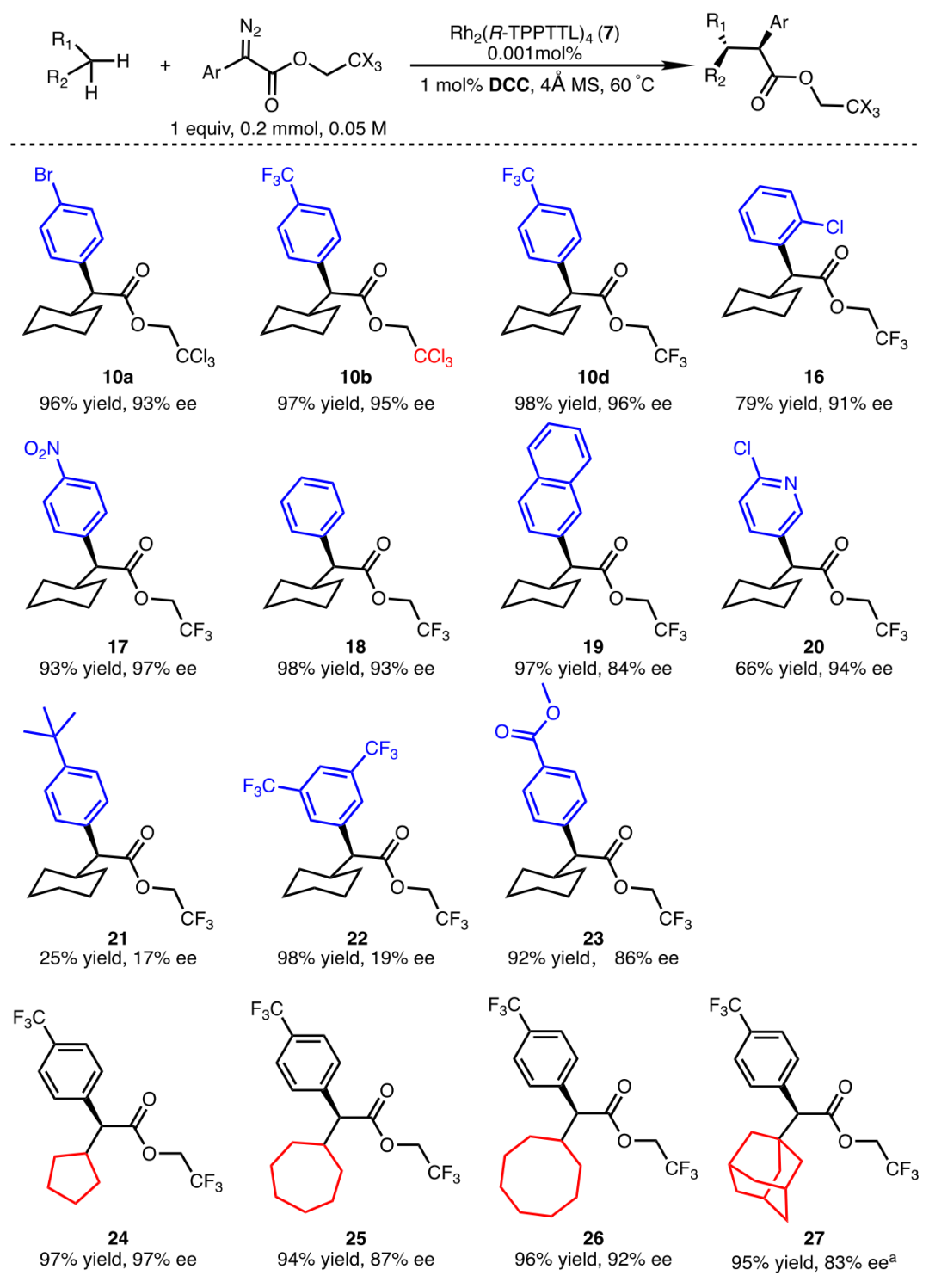
基于动力学,对反应条件进行了优化。采用环烷烃作为溶剂可显著提高卡宾捕获效率,使催化剂用量降低一个数量级仍保持高活性。提高温度亦可加快反应速率。此外,引入带吸电子基团的芳基重氮乙酸酯能够增强卡宾亲电性,从而加速速率决定步骤;相反,给电子取代基则显著降低反应效率。
并且研究还发现添加少量N,N′-二环己基碳二亚胺(DCC)可显著提升催化性能。在极低催化剂用量(0.0005 mol%)下,加入DCC后反应可迅速完成,而无添加剂时反应几乎停滞。对比实验表明,DCC可抑制催化剂失活,并维持高周转数。DFT计算显示,DCC通过弱轴向配位与铑卡宾中间体相互作用,改变其电子结构并促进C-H插入,同时其位阻阻止形成副反应中的叶立德,从而区别于会导致催化剂中毒的配体(如吡啶)。
总体而言,该研究通过动力学机制解析与条件优化,揭示了C-H官能化反应中速率控制因素,并提出通过增强卡宾插入步骤与抑制催化剂失活来实现高效催化的新策略,为低负载、高周转数的C-H官能化反应提供了重要指导。
ACS Catal. 2022, 12, 13400.
超高催化效率
极强位点选择性
优异立体控制能力
兼容复杂底物
毕得Rh2(TPPTTL)4催化剂
BD02625362
BD02571380
点击结构查看产品详情
毕得医药
分子砌块产品库
总数14W+种
多、快、好、省
为实验保驾护航
助力医药研发
成为客户最信赖的合作伙伴

所有文章未经授权禁止转载、摘编、复制或建立镜像,违规转载法律必究。
举报邮箱:1002263188@qq.com